病原因子
病原因子とは、微生物が産生する物質であり、その微生物が病原性を発揮するうえで必要とするものです。細菌や真菌、ウイルスなどから様々な病原因子が産生されますが、病原因子の機能を解明することは、「その微生物がそれぞれに特徴的な病態をどのようにして引き起こすのか?」ということを理解することにつながります。数ある病原因子のうち、私たちは特にバルトネラ属細菌の病原因子について研究を進めています。
バルトネラ属細菌が産生する血管新生因子
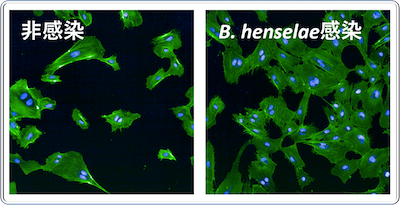
バルトネラ属に分類される細菌はこれまでに40種類以上知られており、人に感染症を起こす重要な菌としてはバルトネラ・ヘンセレ(Bartonella henselae)、バルトネラ・クインタナ(B. quintana)、バルトネラ・バシリフォルミス(B. bacilliformis)の3種類が有名です。ヘンセレは「猫ひっかき病」という動物由来感染症、クインタナはシラミなどを介して感染する「塹壕熱(ざんごうねつ)」、バシリフォルミスは南米アンデス高地の風土病として知られる「カリオン病(オロヤ熱とペルー疣)」の原因菌です。いずれも人(特に免疫不全患の状態の人)に感染すると感染部位の血管を増生させるという他の細菌には見られない性質を持っています。これらの菌は皮膚から感染し血管に到達すると、血管の内腔をおおう血管内皮細胞の増殖を促します。
血管内皮細胞が増えることで毛細血管も増え、結果として血管腫が形成されます。さらに、菌は血管内皮細胞の中まで侵入することで免疫細胞から逃れ、細胞の中で盛んに分裂を繰り返して増殖していきます。すなわち、バルトネラは、隠れ家となる血管内皮細胞を自らの手で増やすことで自身の生存に有利な環境をつくり、結果的に我々ヒトに病気を起こす、という巧みな感染戦略をとる細菌といえます。このような特徴的な性質について、バルトネラからは「血管内皮細胞の細胞増殖を直接促す因子(細胞増殖因子)」が分泌されているということが1990年代後半から指摘されていましたが、その実体については明らかにされていませんでした。
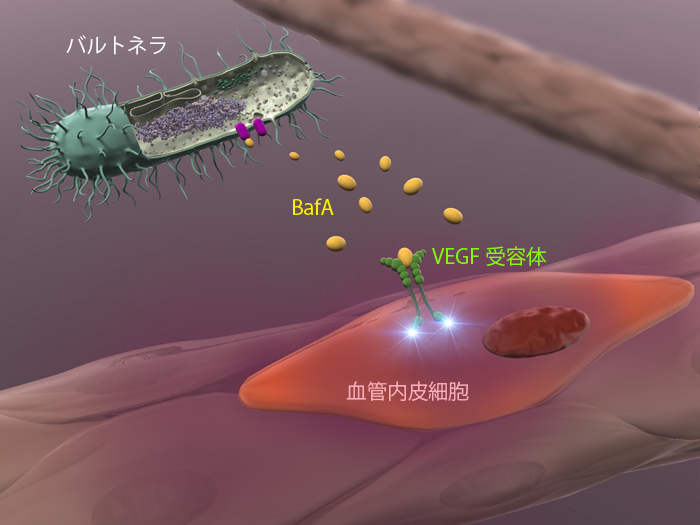
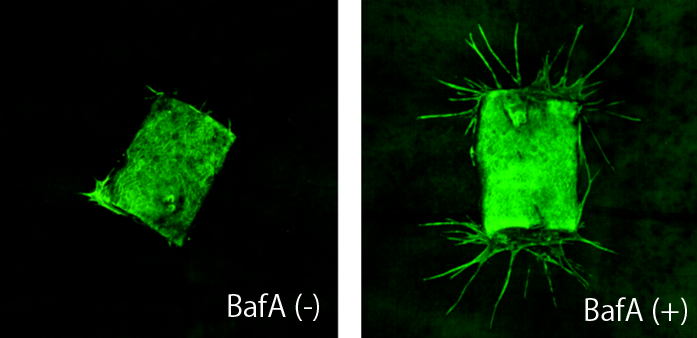
私たちは、この長年正体がつかめていなかったバルトネラの細胞増殖因子を見つけることに成功し、Bartonella angiogenic factor (バルトネラ血管新生因子)の頭文字をとって「BafA」と命名しました。この成果は、2020年にNature Communications誌に論文が掲載されています(https://www.nature.com/articles/s41467-020-17391-2)。BafAの本態はオートトランスポーターと呼ばれるグラム陰性細菌がつくるタンパク質の一種であり、N末端領域の一部が菌体外に分泌されます。分泌されたBafAは、血管内皮細胞の表面に存在する血管内皮増殖因子(VEGF)の受容体の一つVEGFR2に作用します。そして、VEGFR2の下流にあるMAPK-ERK経路というシグナル伝達経路を活性化させることで細胞増殖を促進させます。こうしたBafAの作用の分子メカニズムについても私たちは明らかにしてきました。
また、BafAは細胞増殖だけでなく、既存の血管から新たな血管を発芽・伸張させる「血管新生」を起こすこともマウスを用いた実験でわかりました。このような細菌が産生する血管新生因子は他に報告がなく、BafAは細菌に由来するものとしては世界で初めて発見された血管新生因子といえます。
当初BafAは猫ひっかき病の原因菌であるバルトネラ・ヘンセレから発見されましたが、その後バルトネラ・クインタナやバルトネラ・バシリフォルミスもBafAを産生することもわかりました。バルトネラ・バシリフォルミス由来のBafAについてはその特徴と機能を詳細に解析し、2022年mSphere誌で論文発表しています(https://journals.asm.org/doi/10.1128/msphere.00081-22)。
このように私たちの研究によって、これまで長年実体がつかめていなかったバルトネラ属細菌由来の血管新生因子が特定され、その作用機序も明らかにすることができました。こうした成果は、バルトネラ感染症で血管増殖性病変ができる仕組みやバルトネラの病原発現機構を解明するための大きな一歩になると考えています。また、この新しい血管新生因子であるBafAを虚血性疾患に対する薬に用いたり、再生医療の分野で三次元組織や人工臓器を作製する際の血管ネットワーク構築に用いることはできないかと考え、医療・創薬への応用についても現在研究を進めています。
<本研究に関する発表論文>
- Tsukamoto K, Shinzawa N, Kawai A, Suzuki M, Kidoya H, Takakura N, Yamaguchi H, Kameyama T, Inagaki H, Kurahashi H, Horiguchi Y, Doi Y.
"The Bartonella autotransporter BafA activates the host VEGF pathway to drive angiogenesis"
Nature Communications, 11, 3571 [Full text] - Tsukamoto K, Kumadaki K, Tatematsu K, Suzuki N, Doi Y.
"The Passenger Domain of Bartonella bacilliformis BafA Promotes Endothelial Cell Angiogenesis via the VEGF Receptor Signaling Pathway."
mSphere, 7, e0008122 [Full text]
<プレスリリース・メディア掲載>
- 細菌由来の血管新生因子を世界で初めて発見【日本語】【English】
- Lesion of doom -- how a parasitic bacterium induces blood vessel formation to cause lesions 【 EurekAlert!】
- 日本の研究.com“限りなく客観的なデータ”が導く新発見
<特許出願>
- 「血管新生促進剤」(特願2019-028759)、出願日:2019年2月20日、発明者:塚本健太郎、出願人:学校法人 藤田学園
- 「バルトネラ属細菌に由来するペプチド」(特願2022-33895)、出願日:2022年3月4日、発明者:塚本健太郎、出願人:学校法人 藤田学園
<本研究に関する主な研究助成>
- 文部科学省 科研費 基盤研究(C) 2019年度~2021年度
- 公益財団法人 金原一郎記念医学医療振興財団「第35回基礎医学医療研究助成金」
- 公益財団法人 大山健康財団「第47回学術研究助成金」
- 公益財団法人 発酵研究所「2021年度一般研究助成」
- AMED 令和3年度橋渡し研究戦略的推進プログラム シーズA 名古屋大学拠点「A142」
- JST 研究成果展開事業 社会還元加速プログラム(SCORE)大学推進型(拠点都市環境整備型)
- 文部科学省 科研費 基盤研究(C) 2022年度~2024年度
<本研究に関するお問い合わせ>
塚本 健太郎(講師)
tsuka-k(at)fujita-hu.ac.jp ※(at)を@に変換して下さい。