
脳腫瘍に関する生物学・遺伝学・代謝学的特性についての基礎的研究
廣瀬 雄一 教授
(1)化学療法剤に対するグリオーマ細胞の生物学的反応の解明
代表的な原発性脳腫瘍であるグリオーマは、その浸潤的発育様式のため、重篤な神経脱落症状を呈すること無く外科的に根治することは、極めて困難です。したがって放射線療法、化学療法といった補助療法の施行が必要とされますが、現状ではこれらの治療法を併用しても再発することが多く、有効な補助療法の開発が望まれています。一方、化学療法剤の多くはDNA損傷を起こすことで腫瘍細胞を死滅させることを目的として使われますが、これらの薬剤がグリオーマ細胞内にどのような生物学的反応を惹起するかについては十分には解明されておらず、グリオーマ細胞に関する細胞生物学的知見の不足が抗グリオーマ治療の発達の遅れの一因であるとも言えます。こうした考えに則って、我々は脳腫瘍学におけるtranslational researchの意義を重視し、特に化学療法剤に対するグリオーマの細胞生物学を研究しています。具体的には、化学療法剤で培養グリオーマ細胞を処理して、それに反応して活性の変化する細胞周期制御タンパク、ストレス応答性タンパク、DNA修復関連蛋白などの動向を解析し、その生物学的意義を解明すると共に、治療耐性への関与を研究しています。また、実際に摘出した標本を用いて初発時と再発時の比較を行うことで薬剤耐性に関与する因子の同定も行っている。治療耐性に関わる因子については、その活性を臨床応用可能な方法(例えば薬理学的阻害剤)によって修飾することで化学療法剤の効果を増強させる方法の開発、即ち悪性脳腫瘍の治療への標的治療の導入を、培養細胞だけでなく、マウスでの脳腫瘍移植モデルを用いて試みています。
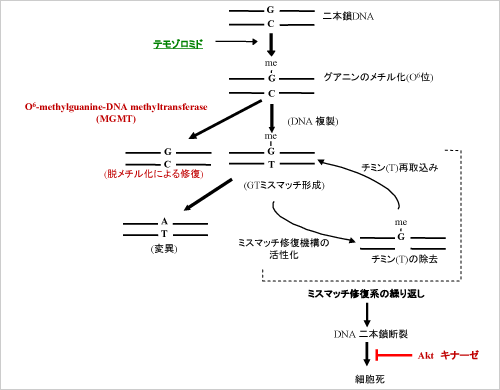
図1:化学療法剤に対する細胞内反応の解明
(関連論文)
- Ohba S, Yamashiro K, Hirose Y. Inhibition of DNA Repair in Combination with Temozolomide or Dianhydrogalactiol Overcomes Temozolomide-Resistant Glioma Cells. Cancers (Basel). 2021 May 24;13(11):2570
- Yamashiro K, Nakao K, Ohba S, Hirose Y. Human Glioma Cells Acquire Temozolomide Resistance After Repeated Drug Exposure Via DNA Mismatch Repair Dysfunction. Anticancer Res. 2020 Mar;40(3):1315-1323.
(2)脳腫瘍の遺伝学的解析
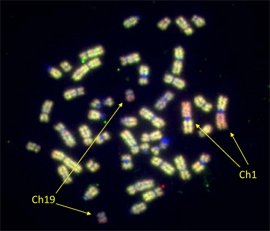
図2:Oligodendroglioma における1p/19q
供欠失の解析
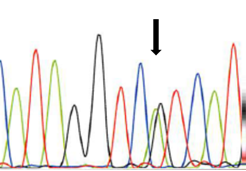
図3:IDH1の塩基配列 (→が変異部)
脳腫瘍の診断は、国際的なworld health organization(WHO)分類に基づいて行われますが、2016年に発表された分類以降、腫瘍の種類によって診断に遺伝子の情報が必要となりました。我々は以前よりホルマリン固定パラフィン包埋切片からのtissue microdissectionを行ない、腫瘍本体部からのみDNAを抽出し、グリオーマの遺伝学的な分類を行ってきました。DNA試料調整に当たっては、これを非特異的に増幅してCGH試料としています。これらの方法の利点は過去に切除され保存されている組織も試料として用いることができる点です。また、凍結した腫瘍組織からDNAを抽出し、腫瘍の遺伝子の塩基配列や、目的とする遺伝子のメチル化を解析しています(ダイレクトシークエンス法、MLPA法、methylation specific PCR)。これらの解析より得られた腫瘍の遺伝学的知見は、病理組織学的所見と合わせることで正確な診断に結びつき、患者の長期的予後の予想を可能とするばかりでなく、適切な補助療法を選択するための助けともなり、臨床的にも有意義な情報を提供できるものです。また、保険適用のがんゲノムパネル検査だけでなく、研究目的での無料のPleSSision-Rapid検査も行っています。これらから得られた結果を診断や治療方針の参考にしています。
(関連論文)
- Kuwahara K, Ohba S, Nakae S, Hattori N, Pareira ES, Yamada S, Sasaki H, Abe M, Hasegawa M, Hirose Y. Clinical, histopathological, and molecular analyses of IDH-wild-type WHO grade II-III gliomas to establish genetic predictors of poor prognosis. Brain Tumor Pathol. 2019 Oct;36(4):135-143
- Hattori N, Hirose Y, Sasaki H, Nakae S, Hayashi S, Ohba S, Adachi K, Hayashi T, Nishiyama Y, Hasegawa M, Abe M. World Health Organization grade II-III astrocytomas consist of genetically distinct tumor lineages. Cancer Sci. 2016 Aug;107(8):1159-64.
(3)脳腫瘍化機構の解明
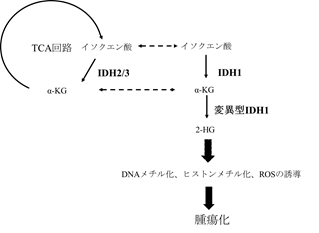
図4:変異型IDHによる腫瘍化機構
2016年以降採用された分子診断において、特に大きな役割を担うものの1つがイソクエン酸脱水素酵素(IDH)の変異であり、グリオーマは変異型IDHの有無により2分されました。
また、IDH変異は、IDH変異型グリオーマのdriver mutationと考えられています。
IDHはイソクエン酸をαケトグルタル酸(α-KG)へと変換させ、変異型IDHはα-KGを2-ハイドロキシグルタル酸(2-HG)へと変換させます。産生された2-HGはα-KG依存性の様々な酵素(DNA demethylaseやhistone demethylase)を阻害し、結果としてDNAやヒストンのメチル化が誘導され、様々な遺伝子の発現に影響を与えることで腫瘍化が生じるとされています。しかしながら腫瘍化の過程にいかなる遺伝学・代謝学的変化が生じるかはまだ十分には解明されていません。
我々はヒトアストロサイトに変異型IDHをはじめとするいくつかの遺伝子を導入することで変異型IDHに依存した腫瘍モデルを形成し、その性質について報告しました。現在、iPS細胞由来の変異型IDH腫瘍化モデルを作成しその遺伝子発現解析を行うことで、腫瘍化機構の解明を目指しています。
(関連論文)
- Ohba S, Mukherjee J, Johannessen TC, Mancini A, Chow TT, Wood M, Jones L, Mazor T, Marshall RE, Viswanath P, Walsh KM, Perry A, Bell RJ, Phillips JJ, Costello JF, Ronen SM, Pieper RO. Mutant IDH1 Expression Drives TERT Promoter Reactivation as Part of the Cellular Transformation Process. Cancer Res. 2016 Nov 15;76(22):6680-6689.
- Ohba S, Mukherjee J, See WL, Pieper RO. Mutant IDH1-driven cellular transformation increases RAD51-mediated homologous recombination and temozolomide resistance. Cancer Res. 2014 Sep 1;74(17):4836-44
(4)脳腫瘍におけるがん代謝を標的とした治療法の開発
がん代謝は、50年以上前にWarburgが唱えましたが、近年再注目され精力的に研究が行われています。がん細胞内の代謝は、正常細胞と異なり、がん細胞が置かれた環境に抵抗し生存に有利な方向に変化しています。それ故、がん細胞特有の代謝の阻害は、従来の化学療法剤と異なった新たな治療法としての役割が期待されます。また、代謝に関与する酵素が、DNAの修復など別の役割を担うことも報告されており、がん代謝の阻害が既存の治療法の効果を高める可能性もあります。
野生型IDH、変異型IDHが代謝と深く関与していることから、IDH変異型グリオーマとIDH野生型のグリオーマにおける代謝の差異がもつ治療標的としての可能性、また実診療において問題となっている化学療法剤耐性腫瘍における代謝の変化と代謝を標的とした治療法の可能性について検証しています。
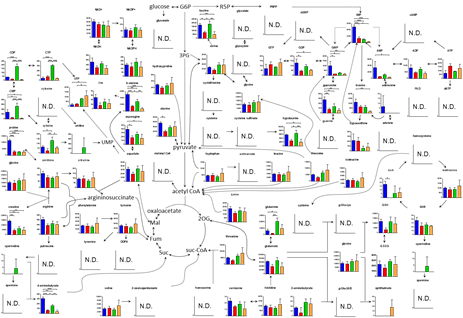
図5:網羅的代謝解析の例
(関連論文)
- Ohba S, Johannessen TA, Chatla K, Yang X, Pieper RO, Mukherjee J. Phosphoglycerate Mutase 1 Activates DNA Damage Repair via Regulation of WIP1 Activity. Cell Rep. 2020 Apr 14;31(2):107518.
- Ohba S, Hirose Y. L-asparaginase and 6-diazo-5-oxo-L-norleucine synergistically inhibit the growth of glioblastoma cells. J Neurooncol. 2020 Feb;146(3):469-475.
(5) Patient-derived xenograft (PDX)モデルを用いた新薬の開発
歴史的に腫瘍の細胞株を用いた実験が行われてきましたが、細胞株では実臨床での腫瘍の不均一性を十分に再現していないことが指摘されています。近年、手術で摘出した腫瘍組織を免疫不全マウスに移植し、より実際の腫瘍に近いものを作成し、それらに対して抗腫瘍薬のスクリーニングテストや腫瘍の性質を解明する解析を行うことが始まっています。当大学でも、脳腫瘍PDXプロジェクトが開始され、今後PDXモデルを用いた解析を行っていきます。
(6)画像解析による脳腫瘍の診断
脳腫瘍には100以上も種類があり、また非腫瘍性病変でも腫瘍に似た画像所見を示すものがあり、画像診断に難渋することがあります。通常のMRIやCTに加え、MRSやperfusion MRI、CESTイメージングなどを用いて、術前の鑑別診断の精度を上げる方法を探索しています。
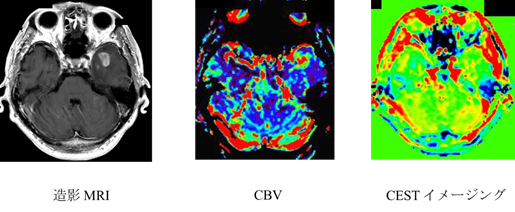
図6:脳腫瘍の特殊画像
(関連論文)
- Kawazoe Y, Ohba S, Murayama K, Nakae S, Nishiyama Y, Abe M, Hasegawa M, Hirose Y. Contrast-Enhanced Magnetic Resonance Imaging, Perfusion Magnetic Resonance Imaging, and 1H-Magnetic Resonance Spectroscopy Distinguish Primary Central Nervous System Vasculitis from Glioblastoma. World Neurosurg. in press
- Kumon M, Nakae S, Murayama K, Kato T, Ohba S, Inamasu J, Yamada S, Abe M, Sasaki H, Ohno Y, Hasegawa M, Kurahashi H, Hirose Y. Myoinositol to Total Choline Ratio in Glioblastomas as a Potential Prognostic Factor in Preoperative Magnetic Resonance Spectroscopy. Neurol Med Chir (Tokyo). 2021 Aug 15;61(8):453-460.
- Nakae S, Murayama K, Sasaki H, Kumon M, Nishiyama Y, Ohba S, Adachi K, Nagahisa S, Hayashi T, Inamasu J, Abe M, Hasegawa M, Hirose Y. Prediction of genetic subgroups in adult supra tentorial gliomas by pre- and intraoperative parameters. J Neurooncol. 2017 Jan;131(2):403-412.
臨床情報、検体、組換えDNAや動物などを用いた研究に関してはそれぞれ該当する委員会の承認を得た上で行っています。また、当大学内だけでなく、国内外の施設とも積極的に共同研究を行い、予後の改善を目的に尽力しています。
