定期報告
定期報告について
特定臨床研究を実施する研究責任医師は、厚生労働大臣に対する定期報告(法第18条関係)を行う義務を有します。
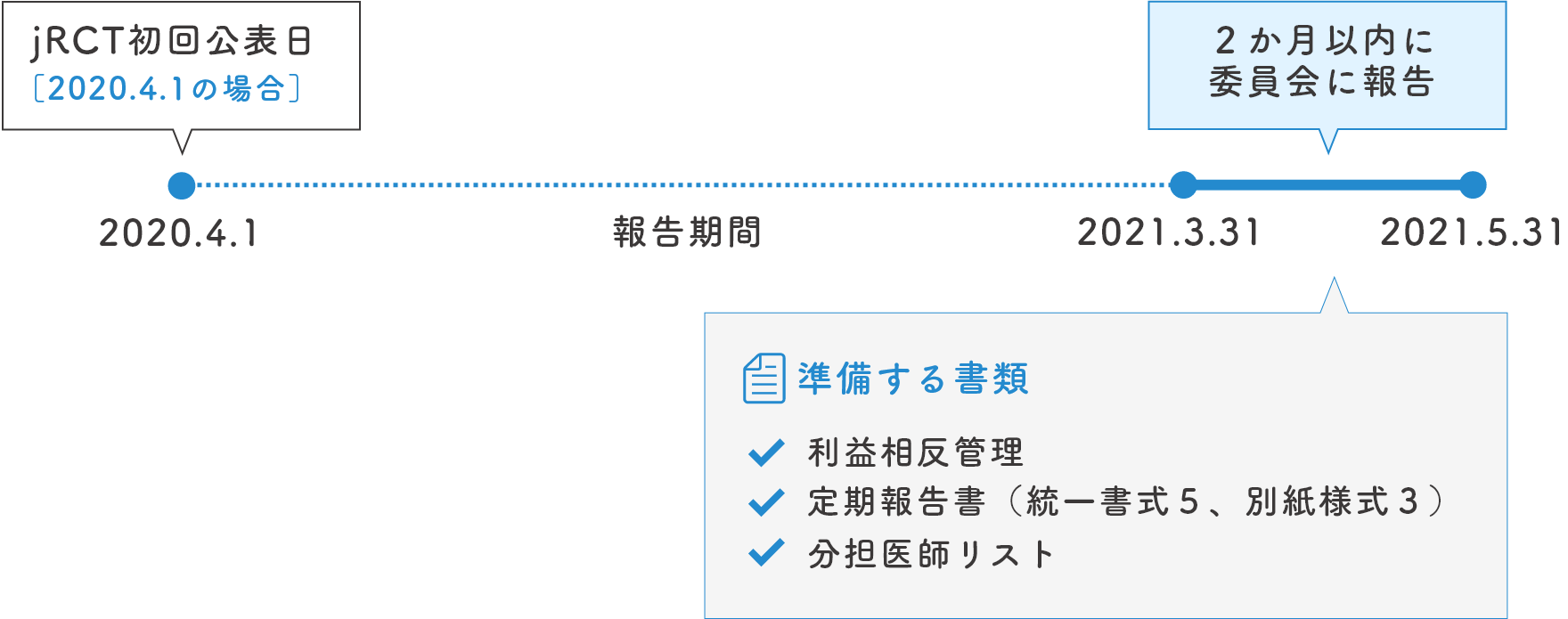
報告時期は、実施計画を厚生労働大臣に提出した日から起算して1年ごと、当該期間満了後2か月以内です。
2.実施医療機関の管理者に報告
申請システムで実施医療機関の管理者に報告します。1で準備した書類を申請システムにアップロードしてください。
報告が受領されると、受領書が発行されます。
実施医療機関毎に受領書の発行方法が異なります。
実施医療機関毎に受領書の発行方法が異なります。
- 藤田医科大学病院・・・システム内で受領書をダウンロードしてください。(ページ一番下の手順を参照のこと。)
- 藤田医科大学ばんたね病院、七栗記念病院、岡崎医療センター・・・報告の受領書の原本を送付いたします。
3.委員会に報告
報告は申請システムより行います。1で準備した書類を申請システムにアップロードしてください。
- 特定臨床研究に参加した対象者*1の数
- 疾病等の発生状況及びその後の経過*2
- 省令又は研究計画書に対する不適合の発生状況及びその後の対応
- 安全性及び科学的妥当性についての評価*3
- 管理が必要な利益相反に関する事項
4.審査結果通知書の発行
原則、審査日から2週間以内に通知いたします。
審査結果通知書が発行されると、申請システムよりメールが届きます。
システム内で審査結果通知書をダウンロードしてください。(ページ一番下の手順を参照のこと。)
システム内で審査結果通知書をダウンロードしてください。(ページ一番下の手順を参照のこと。)
5.(多施設共同研究の場合)各実施医療機関の管理者への報告
申請システムで実施医療機関の管理者に報告します。
統括管理者より受領した書類を、申請システムにアップロードしてください。
統括管理者より受領した書類を、申請システムにアップロードしてください。
報告が受領されると、受領書が発行されます。
実施医療機関毎に受領書の発行方法が異なります。
実施医療機関毎に受領書の発行方法が異なります。
- 藤田医科大学病院・・・システム内で受領書をダウンロードしてください。(ページ一番下の手順を参照のこと。)
- 藤田医科大学ばんたね病院、七栗記念病院、岡崎医療センター・・・報告の受領書の原本を送付いたします。
6.jRCTに登録および厚生労働大臣に提出
研究責任医師(多施設共同研究の場合には統括管理者)は、委員会が意見を述べた日から起算して1月以内にjRCTで定期報告を登録してください。
- 認定臨床研究審査委員会の名称
- 認定臨床研究審査委員会による当該臨床研究の継続の適否
- 特定臨床研究に参加した対象者の数
*1:「対象者の数」については、研究実施期間における実施予定症例数、同意取得症例数、実施症例数、完了症例数、中止症例数及び補償を行った件数を記載
*2:「疾病等の発生状況及びその後の経過」について、既に報告及び審査されているものも含め、臨床研究全体としての疾病等の発生状況を要約て簡潔に記載
*3:「安全性及び科学的妥当性についての評価」とは、疾病等の発生状況及びその後の経過、不適合事案の発生状況及びその後の対応等を含む臨床研究の実施状況並びに当該期間中に発表された研究報告等における当該臨床研究に用いる医薬品等に関連する有効又は無効の情報を踏まえ、当該臨床研究の安全性及び科学的妥当性についての評価について記載
<受領書ダウンロード手順>
- 申請システム 実施許可課題一覧(実施医療機関の管理者に申請)より臨床研究課題を表示する
- 申請履歴 定期報告の表示をクリック
- 画面をスクロールダウンし、下の方にある実施許可書ボタンをクリック
<審査結果通知書ダウンロード手順>
- 申請システム 審査課題一覧(臨床研究審査委員会に申請)より臨床研究課題を表示する
- 申請履歴 定期報告の表示をクリック
- 画面をスクロールダウンし、下の方にある実施許可書ボタンをクリック
