IDH遺伝子変異に応じた脳腫瘍の新たな代謝標的を同定
—グリオーマに対する個別化治療(プレシジョンメディシン)への新展開—
藤田医科大学 脳神経外科学 大場茂生臨床教授、廣瀬雄一教授、放射線医学 村山和宏准教授、医科学研究センター 難病治療学 土田邦博教授、常陸圭介講師、腫瘍医学研究センター 佐谷秀行センター長、慶應義塾大学 平山明由准教授、カリフォルニア大学サンフランシスコ校脳神経外科 Russell Pieper教授らの研究グループは、悪性脳腫瘍である神経膠腫(グリオーマ※1)において、IDH遺伝子変異※2の有無によって異なるアミノ酸代謝※3の脆弱性が存在することを明らかにしました。
グリオーマは、同じ疾患名であっても遺伝子変異の違いによって生物学的特性や治療反応性が大きく異なることが知られています。しかし、これまでIDH変異の有無に応じて「どの代謝経路が治療上の弱点となるのか」については十分に解明されていませんでした。本研究では、細胞実験・動物モデルに加え、130例の臨床MRI/磁気共鳴スペクトロスコピー(MRS)データ解析を組み合わせることで、IDH野生型グリオーマでは「アスパラギン代謝」、IDH変異型グリオーマでは「グルタミン/グルタミン酸代謝」が、それぞれ腫瘍の生存や増殖に重要な役割を果たしており、治療標的として脆弱性を有する可能性が示されました。本研究成果は、グリオーマ治療を遺伝子変異に基づいて最適化する個別化治療(プレシジョンメディシン)の実現に向けた重要な知見であり、将来的な新規治療法開発への応用が期待されます。
本研究成果は、国際学術誌 「Acta Neuropathologica Communications」 に掲載され、2025年11月29日にオンライン版が公開されました。
グリオーマは、同じ疾患名であっても遺伝子変異の違いによって生物学的特性や治療反応性が大きく異なることが知られています。しかし、これまでIDH変異の有無に応じて「どの代謝経路が治療上の弱点となるのか」については十分に解明されていませんでした。本研究では、細胞実験・動物モデルに加え、130例の臨床MRI/磁気共鳴スペクトロスコピー(MRS)データ解析を組み合わせることで、IDH野生型グリオーマでは「アスパラギン代謝」、IDH変異型グリオーマでは「グルタミン/グルタミン酸代謝」が、それぞれ腫瘍の生存や増殖に重要な役割を果たしており、治療標的として脆弱性を有する可能性が示されました。本研究成果は、グリオーマ治療を遺伝子変異に基づいて最適化する個別化治療(プレシジョンメディシン)の実現に向けた重要な知見であり、将来的な新規治療法開発への応用が期待されます。
本研究成果は、国際学術誌 「Acta Neuropathologica Communications」 に掲載され、2025年11月29日にオンライン版が公開されました。
研究成果のポイント
- IDH野生型グリオーマがアスパラギン枯渇に高い感受性を示すことを解明
- IDH変異型グリオーマでは、グルタミン/グルタミン酸代謝系の枯渇に対して脆弱であることを示した
- IDH変異ステータスに基づく代謝標的治療という新たな治療戦略の可能性を提示
背景
グリオーマは代表的な悪性脳腫瘍であり、手術・放射線治療・化学療法を組み合わせた標準治療を行っても、依然として予後は不良です。そのため、新たな治療戦略の確立が強く求められています。近年、IDH遺伝子変異がグリオーマの発生や進展に深く関与していることが明らかとなり、WHO脳腫瘍分類においても重要な診断・分類因子として位置付けられています。IDH変異の有無は、患者の予後や治療反応性に大きな影響を与えることが知られていますが、それぞれの腫瘍に適した分子標的や治療戦略については未解明な部分が多く残されていました。
こうした中、がん細胞のエネルギー産生や物質合成を支える「代謝」に着目した治療戦略が注目されています。腫瘍細胞は正常細胞とは異なる代謝様式に依存していることが多く、その代謝的弱点を標的とすることで、より選択的な治療が可能になると考えられています。
研究手法・研究成果
本研究では、IDH野生型およびIDH変異型グリオーマ細胞を用いた網羅的代謝解析、動物モデルによる治療効果検証、130例の患者データを用いたMRI/MRS解析を組み合わせて検討しました。

図1のように、IDH野生型グリオーマではアスパラギン濃度が、IDH変異型グリオーマではグルタミンおよびグルタミン酸濃度が、それぞれ有意に低下していることが明らかとなりました。
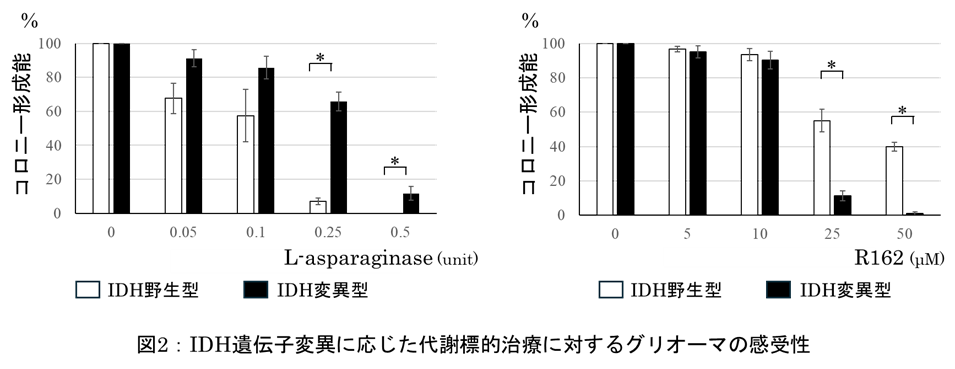
さらに、図2が示すようにIDH野生型グリオーマではアスパラギン代謝への依存性が高く、L-asparaginaseによるアスパラギン枯渇に対して高い感受性を示すことが明らかとなりました。一方、IDH変異型グリオーマでは、グルタミン代謝経路、とくにGLUD1が腫瘍の生存に重要な役割を果たしており、その阻害(R162)によって酸化ストレスが誘導されることが示されました。これらの結果から、IDH遺伝子変異の有無に応じて、標的とすべき代謝経路が明確に異なることが示され、従来の一律な治療戦略とは異なる、新たな治療概念が提示されました。
今後の展開
本研究成果は、グリオーマに対する治療を「一律」ではなく、遺伝子変異に基づいて最適化する個別化医療の基盤となるものです。今後は、既存薬剤の新たな活用や、新規代謝標的治療薬の開発、さらには臨床試験を見据えた検討へと研究を発展させることで、治療抵抗性の高い脳腫瘍に対する新たな治療選択肢の創出が期待されます。
また、本研究で示されたアプローチは、グリオーマに限らず、他のがん種における代謝標的治療の開発にも応用可能な概念であり、今後のがん研究全体への波及効果も期待されます。
用語解説
※1 グリオーマ:脳内のグリア細胞から発生する腫瘍の総称。※2 IDH遺伝子変異:がん細胞の代謝に影響を与える遺伝子変異で、グリオーマの分類や予後と密接に関係する。本研究では、IDH変異の有無によって腫瘍が依存するアミノ酸代謝が異なることを示した。
※3 アミノ酸代謝:細胞がエネルギーや物質合成のためにアミノ酸を利用する仕組み。
文献情報
論文名
Targeting distinct amino acid metabolic vulnerabilities in IDH-mutant and IDH-wildtype gliomas著 者
大場茂生1、平山明由2、寺西隆雄1、常陸圭介3、山口央輝4、村山和宏5、棗田学6、立石健祐7、土田邦博3、脇本浩明8、佐谷秀行9、Russell Pieper10、廣瀬雄一1
所 属
- 藤田医科大学 医学部 脳神経外科学
- 慶應義塾大学 政策・メディア研究科
- 藤田医科大学 医科学研究センター 難病治療学
- 四日市看護医療大学 看護医療学部 臨床検査学科
- 藤田医科大学 医学部 放射線医学
- 新潟大学 脳研究所 腫瘍病態学分野
- 横浜市立大学大学院医学研究科 脳神経外科学
- マサチューセッツ総合病院 ハーバード大学 脳神経外科
- 藤田医科大学 腫瘍医学研究センター
- カリフォルニア大学サンフランシスコ校 脳神経外科


