カルバペネム耐性Acinetobacter baumanniiの β-ラクタム系抗菌薬ヘテロ耐性の分子基盤を解明
本研究成果は、米国微生物学会が出版する学術ジャーナル「mBio」に掲載され、4月8日に公開されました。
研究成果のポイント
- 集団内に少数の抗菌薬耐性傾向の強い菌が存在する「ヘテロ耐性」が治療効果に影響すると示唆されるカルバペネム耐性 Acinetobacter baumannii を対象に、国際協力のもと大規模な臨床分離株解析を実施。
- オメガループにおけるアラニン挿入とR2ループでのアミノ酸置換という特定部位の変異を併せ持つADCバリアントが、難治性グラム陰性菌感染症に用いられるβ-ラクタム系抗菌薬に対する耐性化に寄与することを発見。
- 酵素速度論解析により、薬剤が低濃度でも効率的に分解する性質の獲得を確認。X線結晶構造解析により、R2ループの開閉に基づく薬剤結合制御機構を解明。
背 景
カルバペネム耐性 Acinetobacter baumannii は、複数の抗菌薬が効かないことから治療困難となる症例が報告されている高度耐性菌です。本菌は、世界保健機関(WHO)が定める「優先病原体リスト(Bacterial Priority Pathogens List)」において、初版策定から約10年を経た現在も「最優先(Critical)」に位置付けられています。抗菌薬への高度耐性の背景として、Acinetobacter baumannii が示す高い遺伝的多様性が関与していると考えられています。この代表例が「ヘテロ耐性」です。これは同一集団内に少数の強い抗菌薬耐性を示す菌が混在する状態を指します。このような場合、抗菌薬治療により大部分の菌が死滅したとしても、耐性菌だけが選択的に生存、増殖し、感染症の持続、耐性化につながる可能性が指摘されています。しかし、ヘテロ耐性を支える分子機構には不明な点が多く残されています。加えて、最近の包括的なゲノム解析の結果、Acinetobacter baumanniiの染色体にコードされるADC β-ラクタマーゼには、帰属された酵素で200種類以上、未帰属な酵素も含めると900種類以上のバリアントが存在していることが示され、このADCの多様性と抗菌薬耐性との関連にも注目が集まっていました。研究手法・研究成果
研究グループは、国際的な抗菌薬耐性臨床研究ネットワーク(Antibacterial Resistance Leadership Group: ARLG)内で実施されたカルバペネム耐性 Acinetobacter baumannii を対象とした研究プロジェクト(Study Network of Acinetobacter as a Carbapenem-Resistant Pathogen: SNAP)を通じて、428株の臨床分離株を取得しました。これらの菌株について、抗菌薬cefiderocolの感受性を指標にADCバリアントの比較解析を行いました。Cefiderocolは、多剤耐性グラム陰性菌感染症の治療に用いられるβ-ラクタム系抗菌薬であり、カルバペネム耐性菌に対しても高い活性を示す臨床的に非常に重要な薬剤です。ゲノム解析の結果、428株中に52種類のADCバリアントの存在が確認されました。さらに、cefiderocolに対して耐性傾向が観察されるグループには、ADC-33、ADC-225、およびADC-227の3つのバリアントを有する株が集約されていました。これらのバリアントはいずれもオメガループ218a位にアラニン挿入が観察されました。さらに、ADC-33では菌株間で耐性度に幅がみられましたが、アラニン挿入に加えて292位のバリンがグリシン(ADC-225)またはトリプトファン(ADC-227)に置換されたADC-225やADC-227では、菌株間で一貫して高い耐性傾向が認められました。292位のバリンは基質結合ポケットを構成する重要なアミノ酸です。この部位が構造の小さなグリシンに置換された場合、基質結合ポケットの拡張が生じる可能性が考えられます。一方、側鎖が大きいトリプトファンへの置換は、ポケットを狭める方向の変化をもたらすと予想されました。このようにADC-225とADC-227の292位のアミノ酸置換は、一見相反する方向への変化をもたらすことが予想される一方で、いずれの置換でも耐性が強化されていた点は特に注目すべき結果でした。そこで、基質認識がより不利となると考えられたトリプトファン置換型ADC-227に焦点を当て、より詳細な酵素学的解析および構造解析を行いました。その結果、ADC-227はcefiderocolの低感受性化に加え、同じく難治性グラム陰性菌感染症の治療薬であるceftazidime–avibactam合剤に対して更に高度な耐性を付与することが明らかになりました。さらに、ADC-227はcefiderocolやceftazidimeなどの高世代セファロスポリン系薬剤に対し、低濃度でも効率的に分解活性を示すことが耐性強化の主要因であることがわかりました。構造解析の結果、292位を含むR2ループは、基質認識時に大きく開き、基質結合後には変異トリプトファンが“蓋”のように基質を包み込む動的構造変化を示すことが明らかになりました(図1)。このダイナミックな構造変化が、ADC-227が低濃度下でも高い分解活性を可能にする分子基盤であると考えられます。
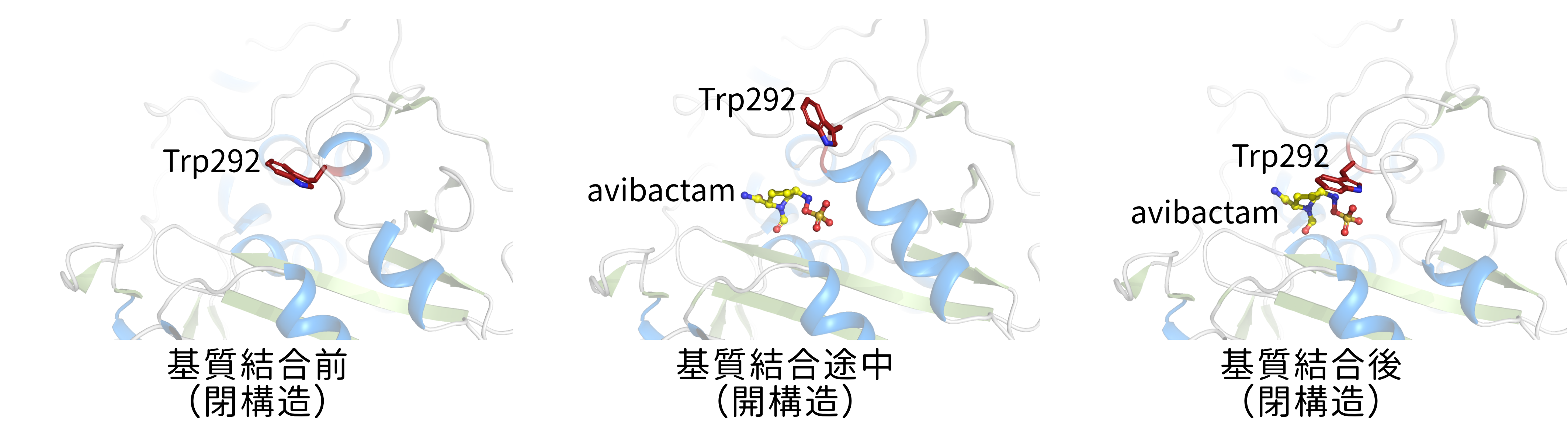
図1 ADC-227の基質結合に伴う構造変化
今後の展開
本研究により、ADC β-ラクタマーゼの292位がβ-ラクタム薬耐性に関わる重要なホットスポットの1つであることが示されました。また、R2ループの動的構造変化という新たな視点は、酵素学的にもβ-ラクタマーゼの基質認識、特異性の理解をさらに深化させる重要な基盤になると考えられます。加えて、今回注目した変異は、カルバペネム系薬剤やAcinetobacter baumannii感染症の治療に特化した最新のβ-ラクタム系抗菌薬sulbactam–durlobactam合剤への耐性に与える影響は限定的であることが示されました。一方で、これらの薬剤の耐性として同定された要因とcefiderocol低感受性化についても一貫性が観察されなかったことから、本研究成果は同クラスの薬剤であっても治療に使える複数の薬剤の存在が現在の難治性細菌感染症治療で重要であることを再認識させる結果となりました。今後、本研究で明らかにした変異を有するADCバリアントの出現動向を分子疫学的に継続的に監視しながら、耐性菌の早期検出や治療戦略の最適化へとつなげていきます。本研究はJSPS科研費(23K06267)、公益財団法人 武田科学振興財団、米国NIH/NIAID [R21AI151362(2024年2月末日で終了)]の助成を受けて実施しました。また、放射光X線回折実験は高エネルギー加速器研究機構放射光科学研究施設共同利用実験(2021G034、2023G081、2025G013)として、Photon Factory BL-17Aにて行いました。
論文情報
論文名
A Val292 substitution combined with an alanine duplication (ADUP) in the Ω loop of ADC β-lactamase confers reduced susceptibility to advanced β-lactam agents including cefiderocol著 者
河合 聡人(共同筆頭著者)1, Christi L. McElheny(共同筆頭著者)2,Ryan K. Shields2,Cesar A. Arias3,David L. Paterson4,Robin Patel5,Robert A. Bonomo6,Vance G. Fowler Jr7,David van Duin8,土井 洋平(責任著者)1,2,9
2. Center for Innovative Antimicrobial Therapy, Division of Infectious Diseases, University of Pittsburgh School of Medicine, Pittsburgh, Pennsylvania, USA
3. Division of Infectious Diseases, Houston Methodist Hospital, Houston., Texas, USA; Center for Infectious Diseases, Houston Methodist Research Institute, Houston, Texas, USA; Department of Medicine, Weill Cornell Medical College, New York, New York, USA
4. ADVANCE-ID, Saw Swee Hock School of Public Health, National University of Singapore, Singapore; Department of Medicine, National University of Singapore, Singapore
5. Division of Clinical Microbiology, Department of Laboratory Medicine and Pathology and Division of Infectious Diseases, Department of Medicine, Mayo Clinic, Rochester, Minnesota, USA
6. Case Western Reserve University-Veteran Affairs Center for Antimicrobial Resistance and Epidemiology (Case VA CARES), Research and Medical Services, Louis Stokes Cleveland Department of Veterans Affairs Medical Center, Cleveland, Ohio, USA; Department of Medicine, Pharmacology, Molecular Biology and Microbiology, and Biochemistry, Case Western Reserve University School of Medicine, Cleveland, Ohio, USA
7. Duke Clinical Research Institute, Duke University, Durham, North Carolina, USA
8. Division of Infectious Diseases, University of North Carolina, Chapel Hill, North Carolina, USA
9. 藤田医科大学 医学部 感染症科
所 属
1. 藤田医科大学 医学部 微生物学講座2. Center for Innovative Antimicrobial Therapy, Division of Infectious Diseases, University of Pittsburgh School of Medicine, Pittsburgh, Pennsylvania, USA
3. Division of Infectious Diseases, Houston Methodist Hospital, Houston., Texas, USA; Center for Infectious Diseases, Houston Methodist Research Institute, Houston, Texas, USA; Department of Medicine, Weill Cornell Medical College, New York, New York, USA
4. ADVANCE-ID, Saw Swee Hock School of Public Health, National University of Singapore, Singapore; Department of Medicine, National University of Singapore, Singapore
5. Division of Clinical Microbiology, Department of Laboratory Medicine and Pathology and Division of Infectious Diseases, Department of Medicine, Mayo Clinic, Rochester, Minnesota, USA
6. Case Western Reserve University-Veteran Affairs Center for Antimicrobial Resistance and Epidemiology (Case VA CARES), Research and Medical Services, Louis Stokes Cleveland Department of Veterans Affairs Medical Center, Cleveland, Ohio, USA; Department of Medicine, Pharmacology, Molecular Biology and Microbiology, and Biochemistry, Case Western Reserve University School of Medicine, Cleveland, Ohio, USA
7. Duke Clinical Research Institute, Duke University, Durham, North Carolina, USA
8. Division of Infectious Diseases, University of North Carolina, Chapel Hill, North Carolina, USA
9. 藤田医科大学 医学部 感染症科


